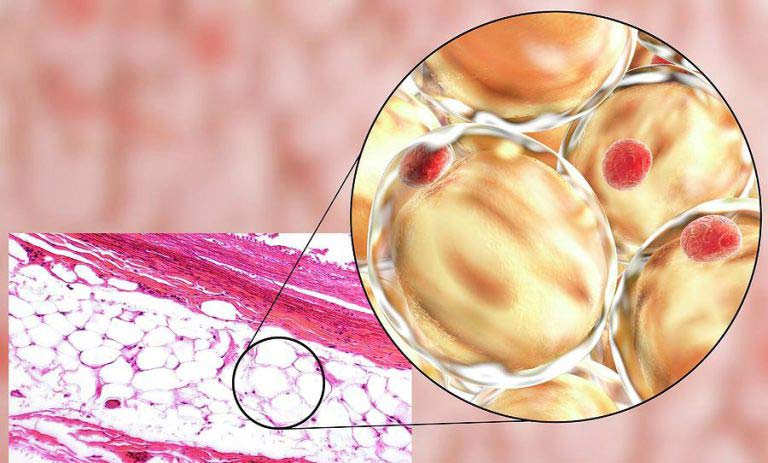
مطالعات در طول دو دهه گذشته بافت چربی را به عنوان یک اندام پویا با چندین فرآیند مهم فیزیولوژیکی نشان داده است. دو طبقه بندی متمایز از بافت چربی وجود دارد: بافت چربی سفید و بافت چربی قهوه ای.
بافت چربی سفید بیشتر چربی موجود در بدن انسان بالغ را تشکیل می دهد و محل حیاتی برای هموستاز انرژی، سیگنال دهی انسولین و عملکرد غدد درون ریز است. بافت چربی قهوه ای عمدتاً مسئول گرمازایی بدون لرز است و چربی قهوه ای به عنوان ذخیره مهم چربی در نوزادان پس از زایمان و در انواع پستانداران شناخته شده است.
چندین مطالعه اخیر با استفاده از توموگرافی انتشار پوزیترون ۱۸F-fluorodeoxyglucose و توموگرافی کامپیوتری نشان دادند که ذخیره بافت چربی قهوه ای در نواحی قفسه سینه و فوق ترقوه انسان بالغ نیز وجود دارد. مطالعات بارباتلی و همکاران نشان داد که سلولهای چربی قهوهای زیر جلدی در موش قابل تشخیص هستند.
انواع سلول های موجود در بافت چربی
بافت چربی شامل انواع مختلفی از سلول ها از جمله سلول های اندوتلیال، سلول های خونی، فیبروبلاست ها، پیش آدیپوسیت ها، ماکروفاژها و سایر سلول های ایمنی است. با این حال، سلول های غالب موجود در بافت چربی، سلول های چربی بالغ هستند. سلول های چربی قهوه ای و سفید به فاکتورهای رونویسی کلیدی برای تمایز از پیش آدیپوسیت ها به سلول های چربی بالغ نیاز دارند.
این تنظیم کننده های رونویسی شامل عوامل حیاتی مانند گیرنده γ فعال شده با تکثیر پراکسی زوم (PPARγ) و سایر خانواده فاکتورهای رونویسی، از جمله پروتئین های CCAAT و C/EBPs، مبدل های سیگنال و فعال کننده های رونویسی (STATs) هستند.
برای کسب اطلاعات بیشتر در مورد فاکتور رونویسی PPARγ اینجا کلیک کنید
برای اطلاع از لیست مارکر های تمایزی نظیر PPARγ – aP2 – FABP4 و… اینجا کلیک کنید
منشا سلول های چربی
درک ما از منشاء سلول های چربی در پنج سال گذشته به طور قابل توجهی تغییر کرده است. در گذشته نه چندان دور پذیرفته شده بود که سلول های چربی قهوه ای و سفید از سلول های پیش ساز مزانشیمی در بافت چربی به وجود می آیند. این ایده با شواهدی که نشان از نیاز سلولهای چربی قهوهای و سفید برای رشد به فاکتور رونویسی PPARγ، تأیید شده بود.
با این حال، این تصور که سلول های قهوه ای و سفید از منشأ مشابهی به وجود می آیند منسوخ شده است. به عنوان مثال، سییل و همکاران نشان دادند که سلول های ذخیره بافت چربی قهوه ای می توانند از سلول های پیش ساز myogenic بیان کننده Myf5 ایجاد شوند.
مطالب مرتبط: جداسازی سلول های بنیادی مزانشیمی از بافت چربی – رده های سلولی در آزمایشگاه کشت سلول
آدیپوژنز Adipogenesis
آدیپوژنز فرآیندی است که در آن سلولهای بنیادی مزانشیمی (MSCs) یا پیش آدیپوسیتها برای کسب ویژگیهای فنوتیپی سلولهای چربی بالغ تمایز مییابند.
آدیپوژنز تشکیل بافت چربی (سلول های چربی) است. چندین گروه نشان دادهاند که سلول های بنیادی چربی های انسانی میتوانند در شرایط آزمایشگاهی با استفاده از سیگنال های القایی حاوی انسولین، متیلیزوبوتیل گزانتین، هیدروکورتیزون یا دگزامتازون در شرایط آزمایشگاهی تمایز پیدا کنند. تحت شرایط تمایز به چربی، سلول های بنیادی چربی در حال تکثیر به پیش آدیپوسیت ها تمایز می یابند.
پیش آدیپوسیت ها مرحله دوم تمایز را پشت سر می گذارند و شروع به تجمع لیپید به شکل واکوئل های کوچک می کنند. سلول های چربی می توانند با تجمع چربی اضافی در طول فرآیند تمایز به بزرگ شدن خود ادامه دهند. آدیپوژنز در شرایط آزمایشگاهی از یک توالی زمانی بسیار منظم پیروی می کند.
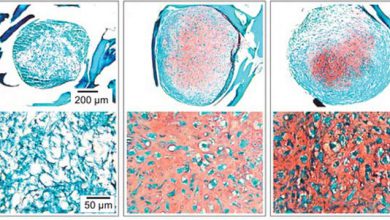
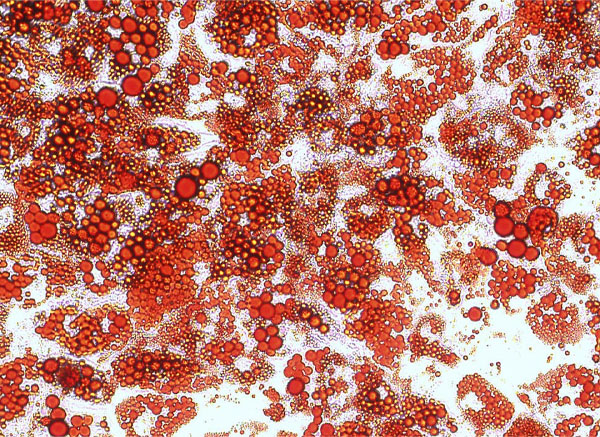
پس از یک هفته تا ۱۰ روز، سلولهای بنیادی چربی ذخایر چربی خنثی درون سلولی خود را افزایش میدهند، این فرآیند را می توان توسط رنگآمیزی Oil Red O یا Nile Red شناسایی نمود، ترشح پروتئین لپتین را افزایش یافته و پروتئین اتصالدهنده اسید چرب، aP2 را بیان میکنند.
در مقایسه با تمایز بسیاری از دودمان های سلولی، تمایز سلول های چربی در شرایط آزمایشگاهی بیشتر ویژگی های کلیدی آدیپوژنز در داخل بدن را داراست. این ویژگی ها شامل تغییرات مورفولوژیکی، توقف رشد سلولی، بیان بسیاری از آنزیمهای لیپوژنیک، تجمع گسترده لیپید، و ایجاد حساسیت به اکثر هورمونهای کلیدی (از جمله انسولین) است که بر این نوع سلول ها تأثیر میگذارند.
مطالب مرتبط: تمایز سلول بنیادی مزانشیمی به استخوان – رنگ آمیزی های بافت شناسی
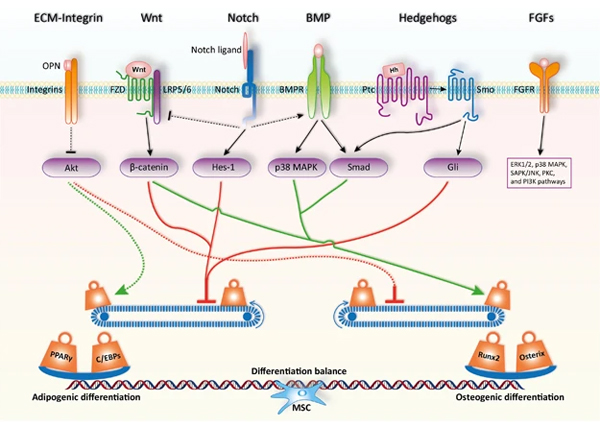
مسیرهای سیگنالینگ در تمایز سلول های بنیادی مزانشیمی به چربی و استخوان
تمایز سلولهای بنیادی مزانشیمی یک فرآیند دو مرحله ای است که شامل تعهد رده سلولی خاص برای تمایز و بلوغ (از اجداد به انواع سلولهای خاص) می شود. مطالعات فشرده در دهههای اخیر نشان دادهاند که تعدادی از مسیرهای سیگنالینگ حیاتی در تنظیم تعهد دودمان سلولهای بنیادی مزانشیمی دخیل هستند، که شامل سیگنال دهی TGFβ BMP – FGFs – Wnt- FGFs- Hh می شود.
خانواده TGFβ/BMPs
ابرخانواده TGFβ از بیش از ۳۰ عضو تشکیل شده است که به طور گسترده در تنظیم تکثیر سلولی، تمایز سلولی و رشد جنینی دخیل هستند. در تمایز سلول های بنیادی مزانشیمی، عملکردهای مختلفی را انجام می دهند که برخی از آنها وابسته به دوز است. برای مثال، BMP4 به تنهایی می تواند تمایز چربی زایی سلول های بنیادی مزانشیمی را تقویت کند، در حالی که BMP2 برای القای تمایز چربی زایی نیاز به همکاری با روزیگلیتازون دارد.
با این حال برای تمایز به سلول های چربی، دوز بالای BMP2 تمایز استخوان زایی و غضروفی C3H10T1/2 را تسریع می کند. مسیر سیگنال دهی TGFβ/BMPs به طور کلی نقش دوگانه ای در تنظیم تمایز به چربی و استخوان سازی سلول های بنیادی مزانشیمی دارد.
خانواده Wnt
خانواده Wnt شامل تعداد زیادی گلیکوپروتئین ترشحی است. Wnt به عنوان یک مسیر سیگنال دهی بسیار حفاظت شده در طول تکامل ارگانیسم های چند سلولی، در بسیاری از فرآیندهای حیاتی بیولوژیکی از جمله توسعه و متابولیسم سلول های بنیادی نقش دارد. لیگاندهای Wnt از طریق اتصال به گیرنده های غشایی FZD و گیرنده های LRP5/6، از طریق جلوگیری از فسفوریلاسیون، β-کاتنین را تثبیت می کنند.
مطالعات اخیر نشان می دهد که سیگنال دهی Wnt نقش مهمی در تنظیم تمایز MSC دارد. فعال شدن سیگنال دهی Wnt برای تسهیل تمایز استخوان زایی و مهار تمایز چربی زایی سلول های بنیادی مزانشیمی گزارش شده است.
مسیر سیگنال دهی Notch
مسیر سیگنال دهی Notch شامل Notch، لیگاند Notch (Delta/Serrate/LAG-2، پروتئین DSL) و CBF1/Su (H)/Lag-1 (CSL، پروتئین اتصال به DNA) است. Notch و لیگاند Notch پروتئین های تک غشایی هستند که شامل ارتباط سلول-سلول برای تنظیم فرآیندهای مختلف تمایز سلولی است. همانطور که توسط مطالعات مدل ۳T3-L1 نشان داده شده است، ناچ مانند یک شمشیر دو لبه، نقش بازدارنده و نقش ضروری مطلق را در تمایز چربی زایی نشان می دهد.
تمایز فیبروبلاستهای مولتی پتانسیل ۳T3-L1 به سلولهای شبه چربی یکی از رایجترین مدلهای آزمایشگاهی مورد استفاده در مطالعه زیستشناسی چربی است.
برای کسب اطلاعات بیشتر در مورد ۳T3-L1 اینجا کلیک کنید
برای اطلاع از انواع آنتی بادی های موجود و دریافت مشاوره رایگان در مورد مسیر های سیگنالینگ انواع آنتی بادی ها اینجا کلیک کنید
مسیر سیگنال دهی Hedgehogs
Hedgehogs ها پروتئین های ترشحی هستند که از سه ارتولوگ تشکیل شده اند: SHh، IHh و DHh. پیش ساز Hedgehogs برای تولید یک قطعه N ترمینال فعال ۱۹ کیلو دالتون، به پروتئین های غشایی Ptc و Smo متصل می شود. اجزای مسیر سیگنالینگ Hedgehog مانند SHh، IHh، و DHh و همچنین Gli در MSCها بیان می شوند. در طول تمایز به چربی سلول های بنیادی مزانشیمی، سیگنال دهی Hedgehogs به دلیل کاهش بیان Gli کاهش می یابد. فعالسازی سیگنال دهی Hedgehogs با مهار بیان PPARγ و C/EBPα و تجمع چربی در سلولهای ۳T3-L1 و C3H10T1/2، تمایز چربیزایی را مسدود می کند. علاوه بر این، مهار Gli می تواند تمایز چربی را افزایش دهد.
سایر مولکول های سیگنال دهی که در تمایز MSC نقش دارند
چندین مسیر سیگنالینگ دیگر نیز در تنظیم تمایز به چربی و استخوان سازی سلول های بنیادی مزانشیمی از جمله FGFs، PDGF، EGF و IGF نقش دارند. نقش آنها در تمایز MSC عمدتاً از طریق تنظیم مسیرهای سیگنالینگ که قبلاً بیان شد، مانند مسیرهای Wnt و TGFβ/BMP اعمال می شود.
FGFs هم در ایجاد چربی و هم در استخوان زایی نقش دارند. خانواده FGF از ۲۳ عضو مرتبط ساختاری تشکیل شده است که تقریباً در همه انواع بافت ها بیان می شوند. پس از اتصال FGF، گیرنده های FGF دیمر می شوند و آبشار سیگنال دهی پایین دستی را راه اندازی می کنند. نشان داده شده است که آبشار سیگنال دهی گیرنده FGF شامل مسیرهای ERK1/2، p38 MAPK، SAPK/JNK، PKC، و PI3K است که همگی نقش مهمی در تنظیم تمایز MSC دارند.
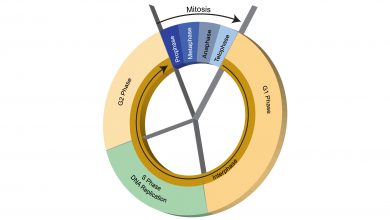
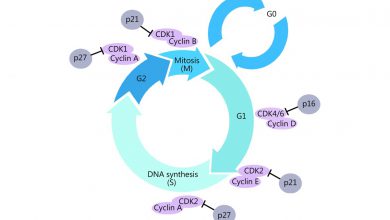
مطالب مرتبط: رده های سلولی در آزمایشگاه کشت سلول– چرخه سلولی و سایکلین ها
خدمات مرتبط: خدمات سلولی – محیط های کشت تمایزی – انجام تکنیک وسترن بلات و الایزا با بانکی غنی از انواع آنتی بادی